- Autor Stanley Ellington ellington@answers-business.com.
- Public 2023-12-16 00:21.
- Ostatnio zmodyfikowany 2025-01-22 16:10.
Różne pochodne kwasu karboksylowego mają bardzo różne reaktywności, chlorki i bromki acylu są najbardziej reaktywne i amidy najmniej reaktywny, jak zaznaczono w poniższej uporządkowanej jakościowo liście. Zmiana reaktywności jest dramatyczna.
Dlaczego więc bezwodniki są bardziej reaktywne niż kwasy karboksylowe?
Bezwodniki są mniej stabilne, ponieważ oddanie elektronów jednej grupie karbonylowej konkuruje z oddaniem elektronów drugiej grupie karbonylowej. Zatem w porównaniu do estrów, gdzie atom tlenu wymaga tylko stabilizacji jednej grupy karbonylowej, bezwodniki są bardziej reaktywny niż estry.
Poza powyższym, który jest bardziej reaktywnym kwasem karboksylowym lub estrem? Na przykład w podstawieniu nukleofilowym, wtedy ester jest bardziej reaktywny niż kwas karboksylowy . Powód jest taki, że estry mają lepsze grupy opuszczające niż grupa hydroksylowa kwas karboksylowy . A ponieważ to jest kwas karboksylowy , istnieje duże prawdopodobieństwo, że będzie to karboksylan (zdeprotonowany) w swojej naturalnej postaci.
Odpowiednio, jakie są pochodne kwasu karboksylowego?
Grupy funkcyjne w sercu tego rozdziału to pochodne kwasu karboksylowego : zawierają kwasy karboksylowe sami, karboksylany (deprotonowane) kwasy karboksylowe ), amidy, estry, tioestry i fosforany acylu. Estry i amidy cykliczne określane są odpowiednio jako laktony i laktamy.
Jakie są cztery pochodne kwasu karboksylowego?
Chociaż znanych jest wiele rodzajów pochodnych kwasu karboksylowego, skupimy się tylko na czterech: halogenkach kwasowych, bezwodnikach kwasowych, estry i amidy.
Zalecana:
Jaka jest różnica między cyklem Krebsa a cyklem kwasu cytrynowego?
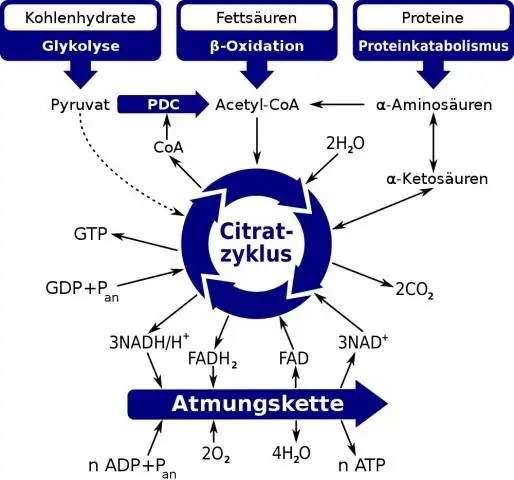
Główna różnica między glikolizą a cyklem Krebsa to: Glikoliza jest pierwszym etapem procesu oddychania i zachodzi w cytoplazmie komórki. Z kolei cykl Kreba lub cykl kwasu cytrynowego obejmuje utlenianie acetylo-CoA do CO2 i H2O
Jakie jest zastosowanie kwasu karboksylowego?
Pochodne kwasu karboksylowego mają różnorodne zastosowania. Na przykład kwas mrówkowy, najprostszy kwas karboksylowy, oprócz zastosowania jako środek dezynfekujący, jest stosowany w obróbce tekstyliów i jako środek redukujący kwasowość. Kwas octowy jest szeroko stosowany w produkcji tworzyw celulozowych i estrów
Jakie są właściwości fizyczne i chemiczne kwasu karboksylowego?

Kwasy karboksylowe mają wysokie temperatury wrzenia w porównaniu z innymi substancjami o porównywalnej masie molowej. Temperatura wrzenia wzrasta wraz z masą molową. Kwasy karboksylowe zawierające od jednego do czterech atomów węgla są całkowicie mieszalne z wodą. Rozpuszczalność maleje wraz z masą molową
Dlaczego kształt krzywej miareczkowania różnił się w przypadku miareczkowania mocnego kwasu vs mocnej zasady i słabego kwasu vs mocnej zasady?

Ogólny kształt krzywej miareczkowania jest taki sam, ale pH w punkcie równoważnikowym jest inne. W miareczkowaniu słabym kwasem i mocną zasadą pH jest większe niż 7 w punkcie równoważnikowym. W miareczkowaniu silnym kwasowo-słabozasadowym pH jest mniejsze niż 7 w punkcie równoważnikowym
Jaka jest zasadowość kwasu octowego?

Kwas octowy zawiera 1 wymienny jon wodorowy na cząsteczkę kwasu lub można powiedzieć, że wytwarza tylko jeden jon wodorowy na cząsteczkę kwasu. Stąd zasadowość kwasu octowego wynosi 1 lub jest to kwas jednozasadowy
